lunes, 25 de agosto de 2014
Forma Rápida de Aprender
Publicado por
Unknown
en
15:56
0
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
elementos,
propiedades,
quimica,
tabla
Quimica
Publicado por
Unknown
en
15:54
0
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
afinidad,
electronegatividad,
grupo,
ionizacion,
metalico,
periodo,
radio,
tablaperioidica
domingo, 24 de agosto de 2014
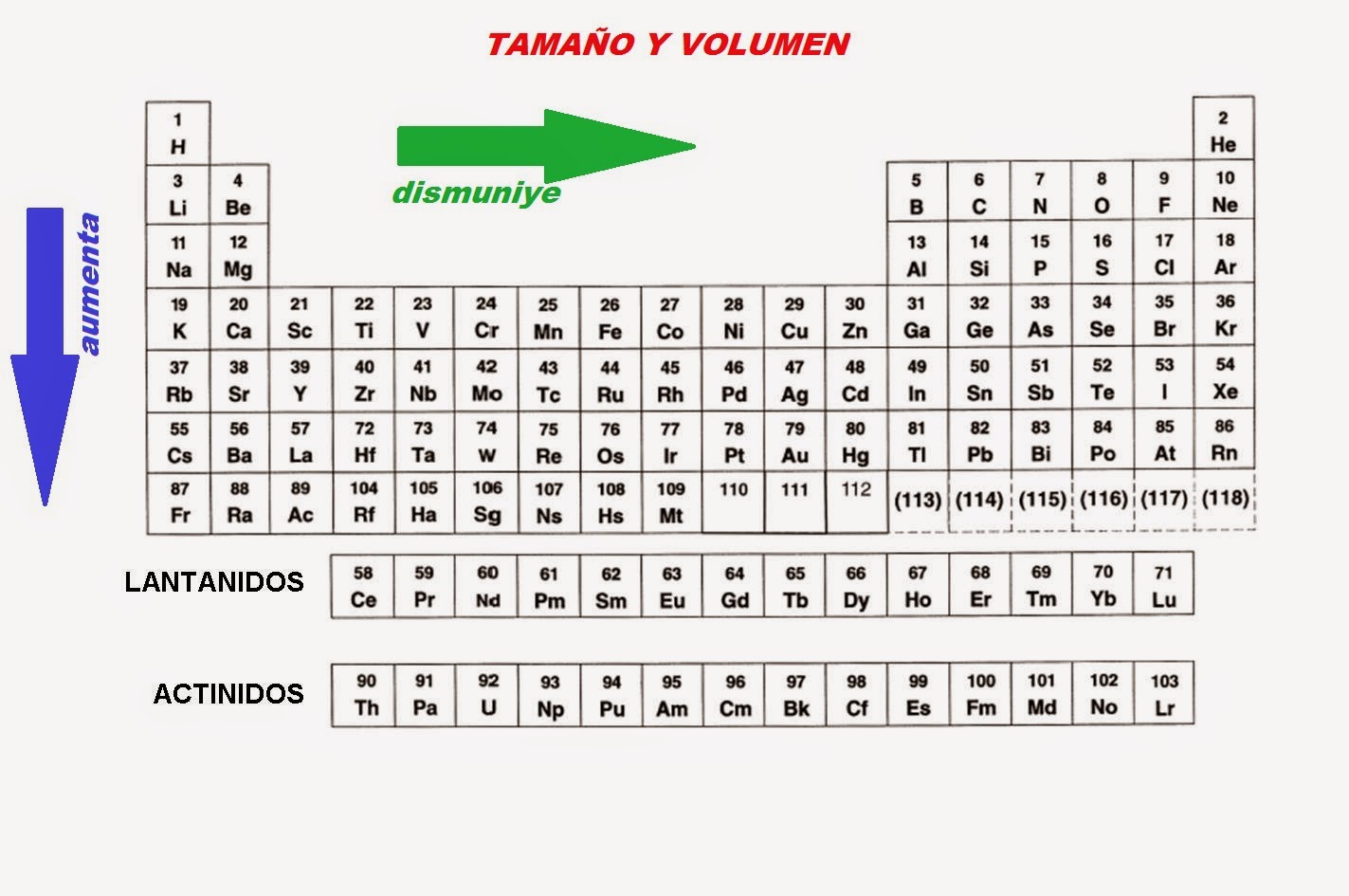
Tamaño y Volumen
Los elementos ubicados en la tabla periódica también tienen una relación con su tamaño y su volumen por las siguientes razones:
1. En el periodo el tamaño de un elemento disminuirá de izquierda a derecha porque si aumenta el numero atómico sus electrones aumentaran y por lo tanto también aumentaran sus protones presentes en el núcleo y entre mas protones tenga un átomo mas fuerza de atracción de los electrones al núcleo existirá.
2. en el grupo aumentara de arriba hacia abajo porque si un átomo tiene mas niveles su tamaño atómico sera mayor como por ejemplo un elemento que tenga 5 niveles tendrá mayor tamaño y volumen que un elemento de niveles 4, 3 ,2 ,1.
1. En el periodo el tamaño de un elemento disminuirá de izquierda a derecha porque si aumenta el numero atómico sus electrones aumentaran y por lo tanto también aumentaran sus protones presentes en el núcleo y entre mas protones tenga un átomo mas fuerza de atracción de los electrones al núcleo existirá.
2. en el grupo aumentara de arriba hacia abajo porque si un átomo tiene mas niveles su tamaño atómico sera mayor como por ejemplo un elemento que tenga 5 niveles tendrá mayor tamaño y volumen que un elemento de niveles 4, 3 ,2 ,1.
Publicado por
Unknown
en
19:26
0
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
numeroatomico,
radio,
tamaño,
volumen
sábado, 23 de agosto de 2014
Potencial de ionizacion
El potencial de ionización es la energía requerida para quitar a un átomo, un electrón de valencia.
como se mira en la tabla periódica
"periodo" aumenta de izquierda a derecha y en el "grupo"
aumenta de abajo hacia arriba esto se debe a:
1. entre el electrón este mas cerca al
núcleo, este núcleo atraerá con mas fuerza al electrón por eso el
potencial de ionización en los grupos aumenta de abajo hacia arriba porque los
niveles de un átomo son menos y entonces mas fuerza de atracción existirá.
2. de izquierda a derecha aumentara porque
si el numero atómico crece sus electrones también y por lo tanto el
protones aumentaran entonces entre mas protones, mas fuerza de atracción habrá
y por lo tanto la energía de ionización sera mayor.
Publicado por
Unknown
en
21:22
2
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
electrones,
energia,
ionizacion,
protones
Electronegatividad
La electronegatividad es sencillamente la fuerza de atracción que tienen los electrones al formar enlaces. esta propiedad también es importante tenerla en cuenta en la formación de compuestos químicos ya que sabremos que clase de compuesto se forma en la unión de los elementos.
La electronegatividad en la tabla periódica "periodo" aumenta de izquierda a derecha y en los "grupos" de arriba hacia abajo disminuye, se lo puede explicar por las siguientes razones:
1. los elementos no metálicos son los mas electronegativos de la tabla periódica porque quieren alcanzar estabilidad electrónica y como están en la derecha de la tabla entonces hacia ese lado aumentara.
2. los elementos metálicos son electropositivos pues para ellos es mas fácil regalar electrones para alcanzar estabilidad electrónica.
3. el Flúor es el elemento mas electronegativo de la tabla periódica "4.0" y el Francio es el menos electronegativo "0.7".
4. Los gases nobles no tienen electronegatividad porque ellos ya tienen estabilidad electrónica.
La electronegatividad en la tabla periódica "periodo" aumenta de izquierda a derecha y en los "grupos" de arriba hacia abajo disminuye, se lo puede explicar por las siguientes razones:
1. los elementos no metálicos son los mas electronegativos de la tabla periódica porque quieren alcanzar estabilidad electrónica y como están en la derecha de la tabla entonces hacia ese lado aumentara.
2. los elementos metálicos son electropositivos pues para ellos es mas fácil regalar electrones para alcanzar estabilidad electrónica.
3. el Flúor es el elemento mas electronegativo de la tabla periódica "4.0" y el Francio es el menos electronegativo "0.7".
4. Los gases nobles no tienen electronegatividad porque ellos ya tienen estabilidad electrónica.
Publicado por
Unknown
en
20:52
0
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
electronegatividad,
electropositivo,
enlaces,
nometales
Afinidad Electronica
Algunas caracteristicas de la afinidad electronica son:
1.No presentan un aumento o disminucion de forma ordenada dentro de la tabla periodica, mas bien en forma desordenada.
2.Los elementos que presentan energias mas negativas son los halogenos (VIIA) debido a que la capacidad de estos elementos es muy alta.
3.La electroafinidad aumenta cuando el tamaño del atomo disminuye
Publicado por
Unknown
en
20:52
1 comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Carácter metálico
El carácter metálico como su nombre lo indica "metal" consiste en identificar un elemento metálico de un no metálico por las siguiente razones:
1. los elementos metálicos son maleables, tienen brillo, tienen dureza.
2. los elementos metálicos les gusta regalar electrones son cationes o electropositivos porque para ellos es mas fácil alcanzar estabilidad electrónica regalando sus electrones de valencia que recibir
3. en la tabla periódica se ubican en la parte izquierda por eso aumenta el carácter.
4. en el grupo aumenta de arriba hacia abajo porque la electronegatividad es menor ya que se podría decir que son electropositivos como el "Francio".
5. un ejemplo seria el calcio que tiene 2 electrones de valencia y para alcanzar estabilidad electrónica mejor es regalarlos que recibir 6 electrones.
Publicado por
Unknown
en
16:16
1 comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook

Etiquetas:
electrones,
metales,
metalico,
tabla
TENER EN CUENTA
las propiedades de la tabla periódica son propiedades de los mismos elementos químicos solo que se necesitan saber para poder ordenarlos de la mejor manera y para que no sea dura su comprensión como por ejemplo:
-agrupar en un lado los metales y en otro lado los no metales
- tener encuenta la electronegatividad y colocar los elementos de forma ascendente de menor a mayor.
los conceptos que se miren a continuación pertenecen a las mas principales propiedades de la tabla periódica existen mas que las de este blog pero no son tan fundamentales como las siguientes propiedades.
Publicado por
Unknown
en
15:59
0
comentarios
Enviar por correo electrónico
Escribe un blog
Compartir en X
Compartir con Facebook


.jpg)







